Условие задачи:
Надувной шарик, заполненный гелием, удерживают на нити. Найдите натяжение нити, если масса оболочки шарика 2 г, объем 3 л, давление гелия 104 кПа, температура 27° C. Плотность воздуха 1,3 кг/м3.
Задача №4.2.81 из «Сборника задач для подготовки к вступительным экзаменам по физике УГНТУ»
Дано:
\(m_{об}=2\) г, \(V=3\) л, \(p=104\) кПа, \(t=27^\circ\) C, \(\rho_{в}=1,3\) кг/м3, \(T_н-?\)
Решение задачи:
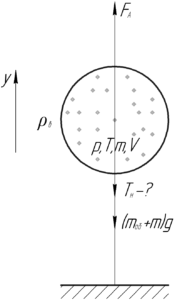 На шарик действуют три силы: сила Архимеда \(F_А\), сила тяжести шарика и гелия \(\left( {{m_{об}} + m} \right)g\) и сила натяжения нити \(T_н\). Надувной шарик находится в равновесии, запишем первый закон Ньютона в проекции на ось \(y\):
На шарик действуют три силы: сила Архимеда \(F_А\), сила тяжести шарика и гелия \(\left( {{m_{об}} + m} \right)g\) и сила натяжения нити \(T_н\). Надувной шарик находится в равновесии, запишем первый закон Ньютона в проекции на ось \(y\):
\[{F_А} — {T_н} — \left( {{m_{об}} + m} \right)g = 0\]
Выразим силу натяжения нити \(T_н\), которую нужно найти по условию задачи:
\[{T_н} = {F_А} — \left( {{m_{об}} + m} \right)g\;\;\;\;(1)\]
Силу Архимеда \(F_А\) (её ещё называют выталкивающей силой) можно определить по формуле:
\[{F_А} = {\rho _в}gV\;\;\;\;(2)\]
Чтобы определить массу гелия \(m\), содержащуюся в шарике, запишем уравнение Клапейрона-Менделеева для гелия в шарике:
\[pV = \frac{m}{M}RT\]
В этом уравнении \(M\) — молярная масса гелия, равная 0,004 кг/моль. Выразим массу гелия:
\[m = \frac{{pVM}}{{RT}}\;\;\;\;(3)\]
Формула (1) после подстановки в неё выражений (2) и (3) примет такой вид:
\[{T_н} = {\rho _в}gV — \left( {{m_{об}} + \frac{{pVM}}{{RT}}} \right)g\]
\[{T_н} = \left( {{\rho _в}V — {m_{об}} — \frac{{pVM}}{{RT}}} \right)g\]
Переведем массу оболочки \(m_{об}\), объем шарика \(V\) и температуру гелия \(t\) в систему СИ:
\[2\;г = 0,002\;кг\]
\[3\;л = 0,003\;м^3\]
\[27^\circ\;C = 300\;К\]
Посчитаем численный ответ к задаче:
\[{T_н} = \left( {1,3 \cdot 0,003 — 0,002 — \frac{{104 \cdot {{10}^3} \cdot 0,003 \cdot 0,004}}{{8,31 \cdot 300}}} \right) \cdot 10 = 0,014\;Н\]
Ответ: 0,014 Н.
Если Вы не поняли решение и у Вас есть какой-то вопрос или Вы нашли ошибку, то смело оставляйте ниже комментарий.
Смотрите также задачи:
4.2.80 Какой радиус должен иметь наполненный гелием воздушный шар, чтобы он мог подняться
4.2.82 Два баллона с объемами 20 и 10 л соединены длинной тонкой трубкой и содержат 6 моль
4.2.83 Воздушный шар объемом 20 м3, наполненный гелием, поднялся на высоту 180 м за 0,5 минуты

 icodepro.ru
icodepro.ru
Добрый! Гелий — благородный газ, поэтому он одноатомный, и его формула He, а не Не2, . А вот кислород объединяется в двухатомные молекулы, и в следствии этого его формула О2.
В результате молярная масса:
гелия — 4 г/моль
кислорода — 16 * 2 = 32 г/моль
Добрый день. Почему мы взяли малярную массу гелия за 4, а не за 8. По сути в других задачах, мы брали малярную массу кислорода за 32 г/ моль.