Условие задачи:
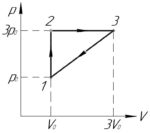 На p-V диаграмме изображен цикл, проводимый с одноатомным идеальным газом. Чему равен коэффициент полезного действия этого цикла?
На p-V диаграмме изображен цикл, проводимый с одноатомным идеальным газом. Чему равен коэффициент полезного действия этого цикла?
Задача №5.5.54 из «Сборника задач для подготовки к вступительным экзаменам по физике УГНТУ»
Дано:
\(\eta-?\)Решение задачи:
 Коэффициент полезного действия цикла \(\eta\) будем находить по формуле:
Коэффициент полезного действия цикла \(\eta\) будем находить по формуле:
\[\eta = \frac{A}{{{Q_н}}}\;\;\;\;(1)\]
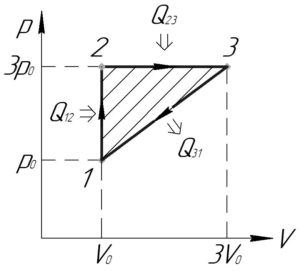
Работу цикла \(A\) численно равна площади фигуры цикла в координатах p-V, при этом если цикл обходится по часовой стрелке, то работа цикла будет положительной (как у нас). Фигура цикла представляет собой прямоугольный треугольник, поэтому:
\[A = \frac{1}{2}\left( {3{p_0} — {p_0}} \right)\left( {3{V_0} — {V_0}} \right)\]
\[A = 2{p_0}{V_0}\;\;\;\;(2)\]
Теперь нужно определить процессы в цикле, в которых теплота подводилась к газу. Запишем первый закон термодинамики:
\[Q = \Delta U + A\;\;\;\;(3)\]
Также запишем формулу для определения изменения внутренней энергии одноатомного идеального газа \(\Delta U\):
\[\Delta U = \frac{3}{2}\nu R\Delta T\;\;\;\;(4)\]
Запишем уравнение Клапейрона-Менделеева для точек 1-3:
\[\left\{ \begin{gathered}
{p_0}{V_0} = \nu R{T_1} \;\;\;\;(5)\hfill \\
3{p_0}{V_0} = \nu R{T_2} \;\;\;\;(6)\hfill \\
3{p_0} \cdot 3{V_0} = \nu R{T_3} \;\;\;\;(7)\hfill \\
\end{gathered} \right.\]
Рассмотрим изохорный процесс 1-2 (\(V=const\)), работа газа \(A_{12}\) в таком процессе равна нулю. Тогда количество теплоты \(Q_{12}\) по формуле (3), учитывая формулу (4), равно:
\[{Q_{12}} = \frac{3}{2}\nu R\Delta {T_{12}}\;\;\;\;(8)\]
Так как давление в процессе 1-2 растёт, значит растёт и температура, то есть \(\Delta T_{12}>0\). Поэтому, согласно формуле (8) \(Q_{12}>0\), то есть теплота в процессе 1-2 подводилась к газу. Учитывая формулы (5) и (6), формула (8) примет вид:
\[{Q_{12}} = \frac{3}{2}\left( {3{p_0}{V_0} — {p_0}{V_0}} \right) = 3{p_0}{V_0}\;\;\;\;(9)\]
Теперь рассмотрим изобарный процесс 2-3 (\(p=const\)). Работа газа \(A_{23}\) в таком процессе равна:
\[{A_{23}} = 3{p_0}\left( {3{V_0} — {V_0}} \right) = 3{p_0} \cdot 3{V_0} — 3{p_0}{V_0}\]
Учитывая уравнения (6) и (7), имеем:
\[{A_{23}} = \nu R\Delta {T_{23}}\]
Количество теплоты \(Q_{23}\) по формуле (3), учитывая формулу (4), равно:
\[{Q_{23}} = \frac{3}{2}\nu R\Delta {T_{23}} + \nu R\Delta {T_{23}}\]
\[{Q_{23}} = \frac{5}{2}\nu R\Delta {T_{23}}\;\;\;\;(10)\]
Так как объем в процессе 2-3 увеличивается, то по закону Гей-Люссака увеличивается и температура (\(\Delta T_{23}>0\)). Поэтому, согласно формуле (10) \(Q_{23}>0\), то есть теплота в процессе 2-3 к газу подводилась. Учитывая формулы (6) и (7), формула (10) примет вид:
\[{Q_{23}} = \frac{5}{2}\left( {3{p_0} \cdot 3{V_0} — 3{p_0}{V_0}} \right) = 15{p_0}{V_0}\;\;\;\;(11)\]
Так как в процессах 1-2 и 2-3 теплота подводится, значит в процессе 3-1 она отводится, так как хотя бы в одном из процессов цикла она должна отводится. Поэтому количество теплоты \(Q_н\), полученное от нагревателя, равно:
\[{Q_н} = {Q_{12}} + {Q_{23}}\]
Подставим в эту формулу выражения (9) и (11), тогда:
\[{Q_н} = 3{p_0}{V_0} + 15{p_0}{V_0}\]
\[{Q_н} = 18{p_0}{V_0}\;\;\;\;(12)\]
В формулу (1) для определения КПД \(\eta\) подставим выражения (2) и (12):
\[\eta = \frac{{2{p_0}{V_0}}}{{18{p_0}{V_0}}} = \frac{2}{{18}} = 0,111 = 11,1\% \]
Ответ: 11,1%.
Если Вы не поняли решение и у Вас есть какой-то вопрос или Вы нашли ошибку, то смело оставляйте ниже комментарий.
Смотрите также задачи:
5.5.53 В некотором процессе газу сообщено 900 Дж теплоты, а его внутренняя энергия
5.5.55 В идеальном тепловом двигателе за счёт каждого килоджоуля энергии, полученной
5.5.56 Холодильник идеального теплового двигателя имеет температуру 27 C. Как изменится

 icodepro.ru
icodepro.ru